ELEMENTOS COMPUESTOS :
Las sustancias puras se clasifican en elementos y compuestos. Los elementos son sustancias simples que no pueden descomponerse por métodos químicos .
MÓLECULAS :
 Las moléculas se representan mediante fórmulas químicas y mediante
modelos. Cuando dos o más átomos iguales o diferentes se unen entre sí
formando una agrupación estable, dan lugar a una molécula. Así, los
gases hidrógeno (H2) y oxígeno (O2) están constituidos por moléculas
diatómicas, en las cuales los dos átomos componentes son esencialmente .
Las moléculas se representan mediante fórmulas químicas y mediante
modelos. Cuando dos o más átomos iguales o diferentes se unen entre sí
formando una agrupación estable, dan lugar a una molécula. Así, los
gases hidrógeno (H2) y oxígeno (O2) están constituidos por moléculas
diatómicas, en las cuales los dos átomos componentes son esencialmente .
 ENLACES IÓNICO :
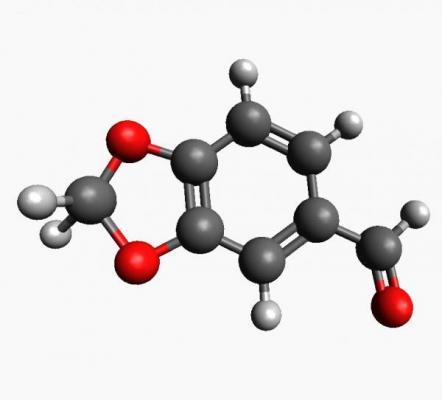
ENLACES IÓNICO :
Un enlace iónico o electrovalente es el resultado de la presencia de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo y otro fuertemente electronegativo. 1Eso se da cuando en el enlace, uno de los átomos capta electrones del otro. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto químico simple, aquí no se fusionan; sino que uno da y otro recibe.
 ENLACE METÁLICO:
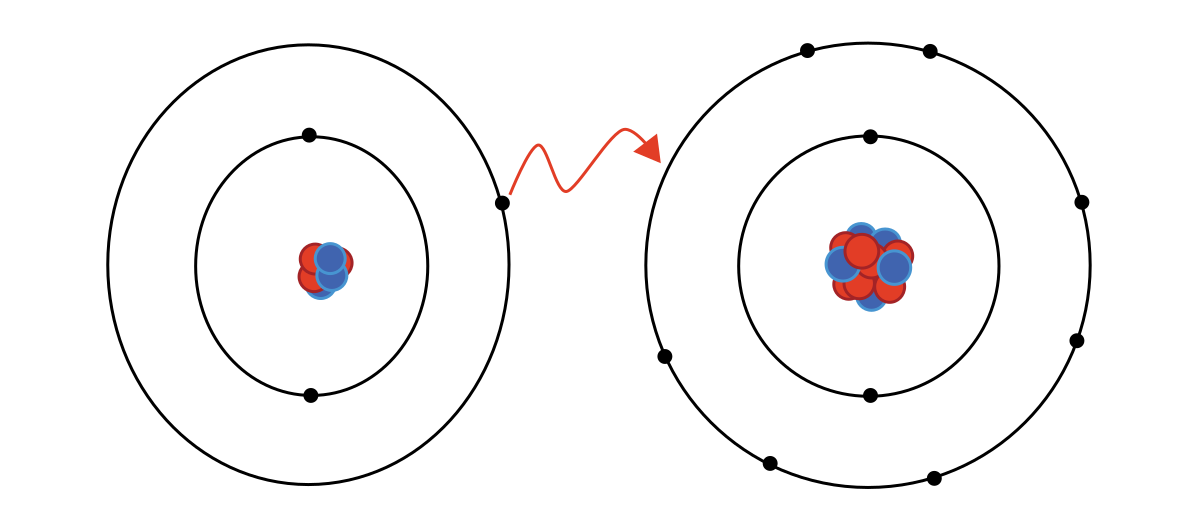
ENLACE METÁLICO:
Un enlace metálico es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí.1
Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de líneas tridimensionales que adquieren estructuras tales como: la típica de empaquetamiento compacto de esferas (hexagonal compacta), cúbica centrada en las caras o la cúbica centrada en el cuerpo.
 ENLACE COVALENTE:
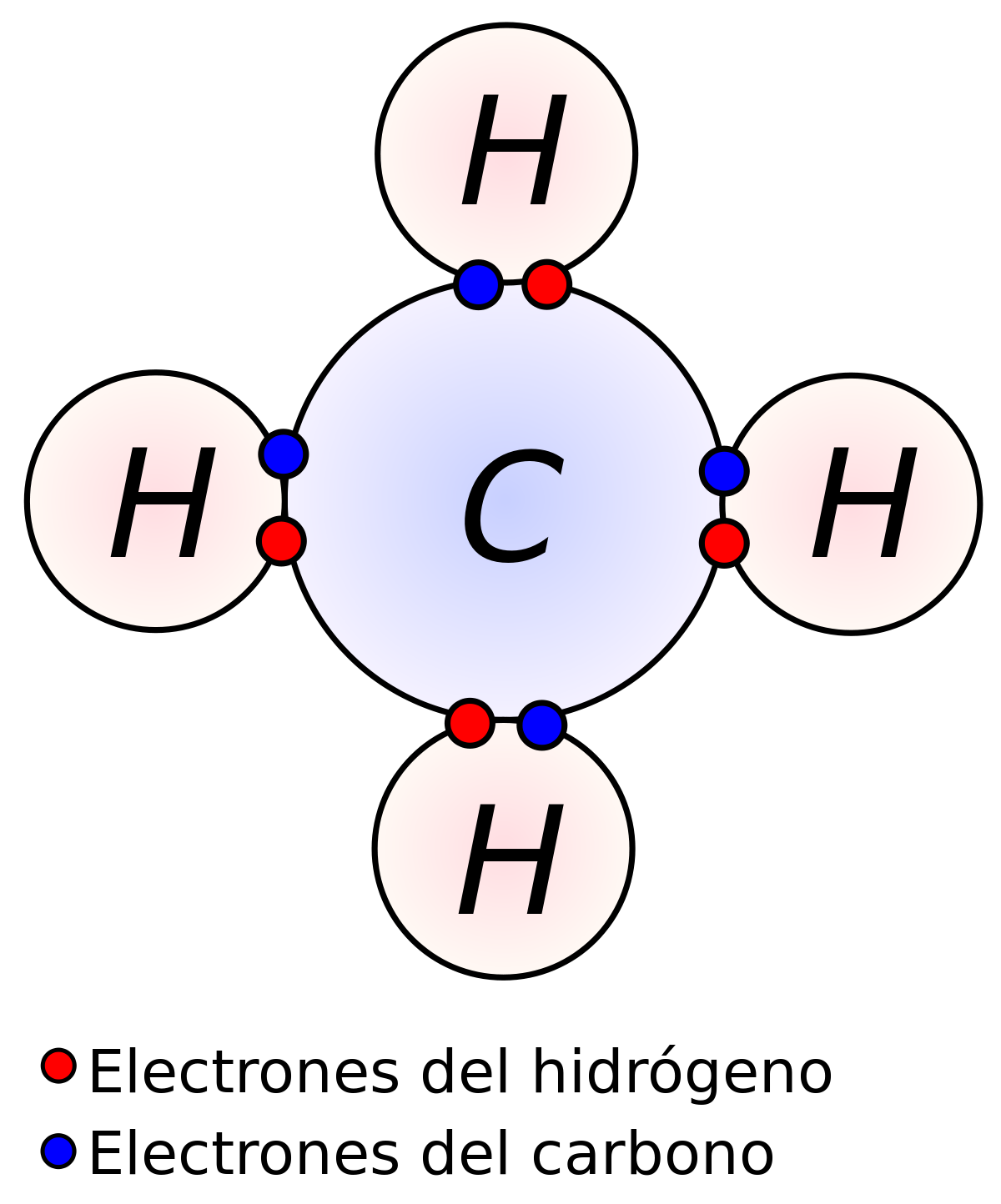
ENLACE COVALENTE:
Un enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel1 (excepto el hidrógeno que alcanza la estabilidad cuando tiene 2 electrones). La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1,7.
 REACCIÓN QUÍMICA:
REACCIÓN QUÍMICA:
NÚMERO DE OXIDACIÓN:
El número de oxidación es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. El número de oxidación es positivo si el átomo pierde electrones, o los comparte con un átomo que tenga tendencia a captarlo.
 EXTEQUIONENTRÍA:
EXTEQUIONENTRÍA:
https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=video&cd=1&cad=rja&uact=8&ved=0ahUKEwjOlMa_wPTfAhVyA2MBHSA_An8QtwIIKTAA&url=https%3A%2F%2Fwww.youtube.com%2Fwatch%3Fv%3DhE2EYR8561Y&usg=AOvVaw2zAIUhBksTMA_X-YoaFcrF
 ENLACES IÓNICO :
ENLACES IÓNICO : ENLACE METÁLICO:
ENLACE METÁLICO:Un enlace metálico es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí.1
Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de líneas tridimensionales que adquieren estructuras tales como: la típica de empaquetamiento compacto de esferas (hexagonal compacta), cúbica centrada en las caras o la cúbica centrada en el cuerpo.
 ENLACE COVALENTE:
ENLACE COVALENTE:Un enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel1 (excepto el hidrógeno que alcanza la estabilidad cuando tiene 2 electrones). La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1,7.
 REACCIÓN QUÍMICA:
REACCIÓN QUÍMICA:NÚMERO DE OXIDACIÓN:
química, la estequiometría (del griego στοιχειον, stoikheion, 'elemento' y μετρον, métrón, 'medida') es el cálculo de las relaciones cuantitativas entre los reactivos y productos en el transcurso de una reacción química.1 Estas relaciones se pueden deducir a partir de la teoría atómica, aunque históricamente se enunciaron sin hacer referencia a la composición de la materia, según distintas leyes y principios.
Comentarios
Publicar un comentario